DİSTROFİN GENİ VE YAŞANAN BOZULMA
Distrofin, insan vücudundaki en uzun gen dizilerinden biridir ve ekzon denilen 79 ana parçadan oluşur. Bu parçalardaki genetik bozulma sonucunda 79 ekzondan bir veya birkaçı temel işlevini yerine getiremezse genin bütünlüğü bozulur ve distrofin üretilemez. Distrofin eksikliği görülen BMD ve DMD hastalarında, sadece düşme veya sert darbeler değil, iskelet kasının doğal kasılma ve gevşeme hareketleri de kasta zedelenmelere yol açar. Kas zedelendiği zaman kandaki CK, myoglobin, hızlı troponin gibi değerlerin arttığı görülür.

Sağlıklı bir insanda distrofin genindeki 79 ekzonun dizilimi aşağıda bulunan şekildeki gibidir. Görüldüğü üzere ekzonların birbirine bağlantı şekilleri de farklılık gösterebilmektedir. Distrofin geninde mutasyona uğrayan ekzonların dışında kalan ekzonlar birleşemez ise, distrofin üretimi durur ve bu durum DMD (Duchenne Musküler Distrofi) olarak adlandırılır. Mutasyona uğrayan ekzonlara rağmen mutasyon dışında kalanlar birbiriyle birleşebilir, kısa ama kısmen fonksiyonel distrofin üretimi devam eder. Bu durumda hasta, DMD (Duchenne) yerine BMD (Becker) olarak adlandırılır. Daha basit bir ifadeyle BMD, DMD’nin hafif seyreden halidir.

EKZON ATLAMA TEDAVİSİ NEDİR?
Ekzon atlama tedavileri, distrofin geninde mutasyona uğrayan ekzonların dışında kalan diğer ekzonların birleştirilmesi prensibine dayanır. Bu tedavi yönteminde birleşmeye uygun olmayan ekzonlar atlatılarak uygun ekzonların birleşmesi hedeflenir. Böylece DMD’nin BMD’ye dönmesi amaçlanır.
Durumu bir örnekle açıklamak gerekirse; ekzon 44 delesyonuna uğramış ve distrofin üretimi görülmeyen bir ekzon dizilimini ele alalım. 45. ekzonun atlanması sonrası geride kalan 43. Ekzon ve 46. Ekzonun birbirine bağlanması için çalışılır.
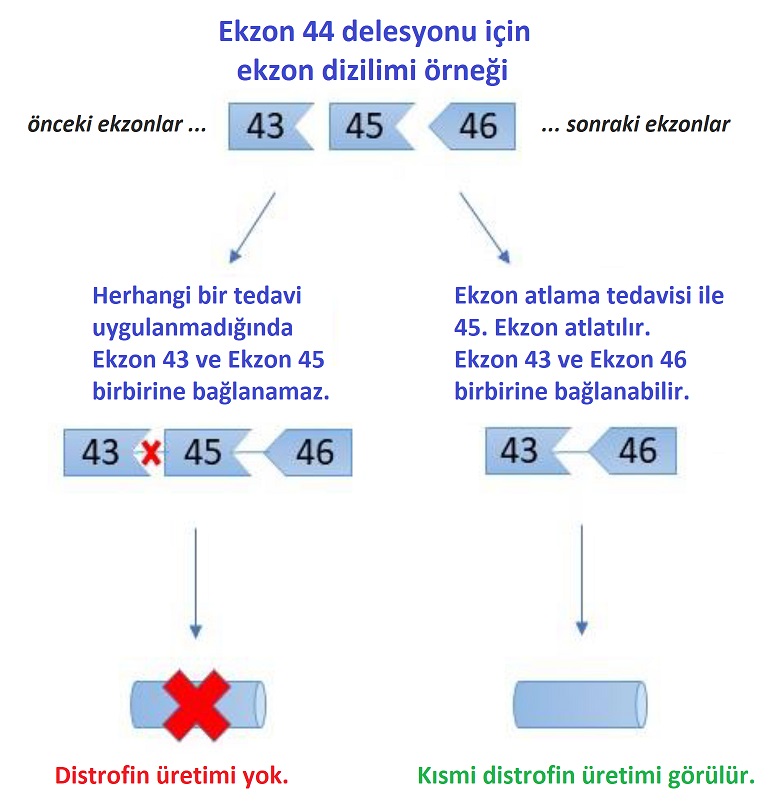
Bu tedaviler, aynı prensibe dayansa da ekzon atlama için kullanılan moleküller ve bu moleküllerin ekzonlar üzerindeki etkileri farklılık gösterirler. Bu sebeple ekzon atlama tedavileri için çalışan ilaç firmalarının uygulamalarında; ilacın düzenli olarak alınacağı periyot (haftalık veya aylık periyotlar), ekzon atlama sonrası üretilecek kısmi distrofin oranı, ilacın hafif veya ciddi yan etkileri birbirinden farklı olacaktır.
DELESYON İÇİN YAPILAN EKZON ATLAMA ÇALIŞMALARI
2022 ve 2023 yıllarında; ekzon atlama tedavilerinde Sarepta ve NS Pharma firmalarının gerek klinik denemeler gerekse ürettiği ilaçlar açısından mevcut deneyimlerinin diğer firmalara göre önde olduğu görülmektedir.
Son yıllarda ise yeni nesil ekzon atlama çalışmaları bir çok farklı firma tarafından yapılmaktadır. Her klinik denemenin başarılı sonuçlanmadığı aşikardır. Başarılı sonuçlananlarının da onay alarak ticari bir ilaca dönüşmesi uzun yıllar alabilmektedir. Ancak teknolojinin ve tıbbi çalışmalardaki gelişmelerin sürekli hız kazanması ve Duchenne üzerinde çalışmalara yönelen birçok farklı firmanın ortaya çıkması olumlu bir gelişme olarak düşünülmelidir.
Ekzon atlama tedavileri, gen terapileri, fibrözü azaltan, kalp ve solunumu koruyan yöntemler gibi Duchenne ve Becker üzerine gerçekleşen tüm çalışmalar için Gelişen Tedaviler ve İlaç Çalışmaları sayfamızı takip edebilirsiniz.
SAREPTA THERAPEUTICS (45, 51, 53)
Sarepta firmasının piyasaya sürdüğü ilk ekzon atlama tedavisi, Ekzon 51 atlama çalışmasıdır. Haftalık doz alımı gerektiren Eteplirsen adlı ilaç, vücuttaki distrofin oranını ortalama olarak % 0.16’dan %0.44’e yükseltmektedir. FDA tarafından 2016 yılında şartlı onay almıştır. Aynı metodolojiye dayanan Ekzon 53 atlama ilacı Golodirsen 2019’da, Ekzon 45 atlama ilacı Casimersen 2021 yılında FDA tarafından şartlı onay almıştır. Amerika dışındaki ülkelerde ise belirgin faydasının kanıtlanması için şart koşulan klinik denemeler devam etmektedir. EMA onayı alınamamış durumdadır.
Özetle, üç ekzon atlama ilacında da distrofin artış oranları, yüzde 1’in altında gerçekleşmiştir.Distrofin artışı düşük, yan etkileri fazla olduğu için dünya genelinde kabul görmemiş, geniş kullanım alanı bulamamıştır. Çalışmalar devam etmektedir.
Sarepta, daha etkili ekzon atlama tedavileri üretmek için çalışmalarını sürdürmüş ve daha fazla taşıma kapasitesine sahip ve PPMO olarak adlandırdığı yeni molekülü sayesinde, ilaç haftalık değil aylık periyotta uygulanacak şekilde düzenlemiştir. MOMENTUM A adı verilen Faz 2 çalışmasının ara verilerinde Eteplirsen’den belirgin şekilde yüksek olarak, % 10.79’luk ortalama ekzon atlama ve % 6.55’lik ortalama distrofin ekspresyonu görüldüğü açıklandı.
2022 Temmuz’da bu yöntemin uygulandığı DMD hastalarında ileri derece magnezyum ve potasyum düşüklüğü görülmesi üzerine FDA’nın bu durum çözülene kadar çalışmaya ara verdirdiği açıklanmıştı. Aynı yılın sonunda, Sarepta’nın bu konudaki incelemeleri sonrası çözüm üretmesi ile beraber denemenin devam ettiği duyuruldu. 2024 Ocak ayında aylık 20 mg/kg doz verilen katılımcılarda 28 hafta sonunda %2.81, 30 mg/kg doz verilen katılımcılarda 28 hafta sonunda % 5.17 distrofin görüldü açıklandı.
2024 Kasım ayında, görülen yüksek distrofin oranlarına rağmen, ilacın karaciğer ve böbrek fonksiyonlarında geri döndürülmez hasarlar oluşturması ve yan etkilerin çözülerek güvenlik kriterlerinin karşılanmaması sebebiyle PPMO çalışmasının sonlandırıldığı açıklandı.
NS PHARMA (44, 53)
Japonya orjinli firmanın, Ekzon 53 atlama ilacı Viltolarsen ABD ve Japonya’da onaylıdır, Avrupa için EMA onay süreci devam etmektedir. Ciddi bir yan etki gözlenmemekle beraber ortalama %6 üzeri distrofin artışı gözlenmiştir. Mevcut onaylı ekzon atlama tedavileri arasında en yüksek etkiyi gösteren ilaç olarak gözükmektedir. Ekzon 53 atlama tedavisinin klinik denemeleri ülkemizde de yürütülmekte olup bu çalışmaya katılan 15’ten fazla çocuğumuz bulunmaktadır.
Firma, ekzon 44 atlama tedavisi için klinik denemededir. Japonya’da 6 çocuk üzerinde ilk defa insan denemesine geçilmiş ve İlk 24 haftalık uygulamanın ardından yapılan ölçümlerde 40 mg/kg doz verilen grupta %10.27, 80 mg/kg doz verilen grupta %15.79 distrofin görülmüştür(https://www.clinicaltrials.gov/study/NCT04129294) NS-089/NCNP-02 kod adlı Faz 2 denemesi global çapta yürütülmektedir.
DYNE THERAPEUTICS (51)
Ekzon 51 atlama için çalışmakta olan firma, ekzon atlama çalışmalarında kullanılan molekülün, iskelet kaslarına daha etkin ulaşmasını sağlayacak bir yöntem üzerinde çalışmaktaydı. Haftalık yerine aylık doz uygulanan klinik denemenin ilk verileri duyurdu.
- 48 katılımcılı Faz 1/2 DYNE-101 çalışmasında, ilacın farklı dozları denendi. İlk 6 ay sonunda ekzon atlama prosedürünün kas hücrelerine ulaştığı, başta karaciğer ve böbrek olmak üzere ciddi yan etki görülmediği açıklandı. (https://www.clinicaltrials.gov/study/NCT05481879)
- Plasebo kontrollü Faz 1/2 DYNE-251 çalışmasında, 5 mg/kg doz uygulanan 4 katılımcının 6 aylık verilerinde ekzon atlamanın görüldüğü kas hücresi sayısı ve distrofin oranının halihazırda Amerika’da şartlı onay alan Eteplirsen’e kıyasla daha etkili olduğu açıklandı. (https://www.clinicaltrials.gov/study/NCT05524883) Doz yükseltilmesinin ardından, 20 mg/kg dozunda tedavi edilen hastalarda ortalama %8,72 normal düzeyde distrofin üretimi gözlemlenmiştir. Fonksiyonel iyileşmeler de 18 aya kadar devam etmiştir. Şirket, 2026 başlarında FDA’ya hızlandırılmış onay başvurusu yapmayı planlamaktadır.
PEPGEN (51)
PepGen, yeni nesil moleküller ile daha etkili ekzon atlama tedavileri üretmeyi amaçladığı PGN-EDO51 çalışması başlattı
- Faz 1 çalışmasında, 32 sağlıklı katılımcıda yapılan denemelerde farklı dozların ekzon atlama sonuçlarına etkisi ve yan etkiler incelenmişti. 10 mg/kg dozun iyi tolere edildiği, 15 mg/kg dozda çeşitli yan etkiler görülse bunların üstesinden gelindiği açıklanmıştı.
- Firma, 8 yaş üzeri DMD hastası 10 katılımcıda Faz 2 çalışmasına başladı ve ilk katılımcıya doz uyguladı. Katılımcılar 5 mg/kg ile başlayarak kontrollü olarak 10 mg/kg ve daha yüksek dozlara geçecekler. Yan etkilerin, ekzon atlamanın görüldüğü hücrelerin ve üretilen distrofin oranının ölçüleceği bu çalışmanın ilk verileri 2024 yılı içerisinde açıklanacak. (https://www.clinicaltrials.gov/study/NCT05524883)
- 2025 Mayıs ayında firma, hedeflenen distrofin seviyelerine ulaşılamaması nedeniyle PGN-EDO51 programını ve tüm DMD odaklı Ar-Ge faaliyetlerini sonlandırmıştır.
BIOMARIN (51)
-
Biomarin tarafından ekzon 51 atlamaya uygun DMD hastaları için geliştirilen BMN 351 adlı antisens oligonükleotid (ASO) terapisi, 4-10 yaş arası çocuklarda yürütülen Faz 1/2 çalışmasıyla aktif olarak devam etmektedir. Çalışma, Türkiye dahil olmak üzere Avrupa’da aktif olarak yürütülmektedir.
WAVE LIFE SCIENCES (53)
-
FORWARD-53 adlı Faz 2 çalışması devam etmektedir. 48 haftalık tedavi sonrası, ortalama %7,8 distrofin üretimi sağlanmıştır. Hastaların %88’inde %5’in üzerinde distrofin artışı gözlemlenmiştir. Fonksiyonel testlerde de anlamlı iyileşmeler rapor edilmiştir.
ENTRADA THERAPEUTICS (44)
-
Ekzon 44 atlamaya yönelik ENTR-601-44 adlı tedavi adayı için FDA, klinik durdurma kararını kaldırmış ve Faz 1b çalışmasının başlatılmasına izin vermiştir.
AVIDITY BIOSCIENCES (44)
-
Ekzon 44 atlamaya uygun DMD hastaları için geliştirilen AOC 1044 adlı tedavi adayı, EXPLORE44 adlı Faz 1/2 çalışmasında değerlendirilmiştir. Çalışmada, kas dokusunda 50 kat daha fazla ilaç birikimi sağlanmış ve distrofin üretiminde anlamlı artışlar gözlemlenmiştir
DUPLİKASYON İÇİN YAPILAN EKZON ATLAMA ÇALIŞMALARI
AUDENTES THERAPEUTICS
DMD’ye sebep olan mutasyon türlerinden biri de duplikasyon, yani 79 ana parçadan oluşan ekzonlardan bir ya da bir kısmının çoklanması sonucu zincirin bozulması ve distrofin üretilmemesidir. DMD hastalarının %10 civarının hastalığa sebep olan mutasyon türü duplikasyondur ve en yaygın duplikasyon türü Ekzon 2 duplikasyonudur.
Audentes Therapeutics firması ve Nationwide Childrens Hastanesi ekibi tarafından yürütülen bir çalışmada, Ekzon 2 duplikasyonu olan hastalar için fazla olan Ekzon 2’lerden birinin atlatılması ile tam uzunlukta distrofin üretilebildiği açıklandı. Uygulanan yöntemin kas hücrelerinin ne kadarına ulaştığını anlamak adına Faz 1 denemesine farklı yaşlardan 3 çocuk alındı. 13 yaşındaki çocukta %1, 8 yaşındaki çocukta %6 ve 7 aylık çocukta %70 distrofin gözlendi. Bu çalışma, gen terapisinde kullanılan AAV virüslerinin taşıyıcı olarak kullanılması yönüyle diğer ekzon atlamalardan farklılık göstermektedir. 2022’de duyurulan bu verilerin atdından yeni çalışmalar ile daha fazla katılımcıda yapılacak çalışmalar planlanmaktadır. (https://www.clinicaltrials.gov/study/NCT04240314)
